미국 항암치료제 시장 진출을 위해 LG화학 종속회사인 LG Chem Life Science Innovation Center, Inc.에 출자하여 Aveo Pharmaceuticals Inc.(이하 Aveo)의 지분 100%를 역삼각합병 방식으로 인수할 것을 10월 18일 공시함.
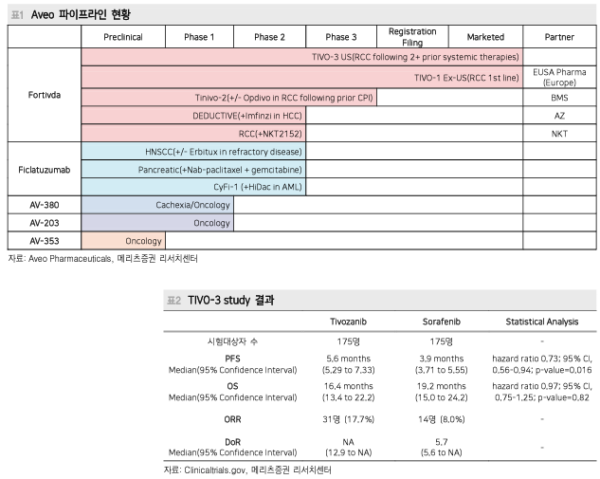
금액은 8,131억원. Aveo는 2001년 창립, 2010년 나스닥에 상장됨. 2017년 유럽 승인(신세포암 1차 치료제), 2021년 미국 승인(신세포암 3차 치료제)되어 시판중인 Fotivda(Tivozanib)와 3상 임상시험 진행중인 두경부암 치료제 Ficlatuzumab 외 3개의 파이프라인을 보유하고 있음.
인수 소식 이후 당일 주가 +42.37% 상승함.
[Fotivda]
2Q22 기준 Aveo 전체 매출액은 2,530만 달러, 이중 Fotivda 매출액은 2,500만 달러. 1Q22에 비해 24% 성장함. 2022년 미국 항암치료 가이드라인(NCCN guideline)에 권고 약제 Category 1(the highest Category recommendation offered by NCCN) 지위 획득 모멘텀으로 2022년 매출액 가이던스 1억 달러에서 1.1억 달러로 상향함.
신세포암은 신장암의 85~90%를 차지하고, 여성과 남성 모두에서 암 발생 10위권 내에 속함. 미국에서 2021년 기준 76,080명이 신장암을 진단받고, 13,780명이 사망했으며 신장암 말기 5년 생존율은 13%에 불과.
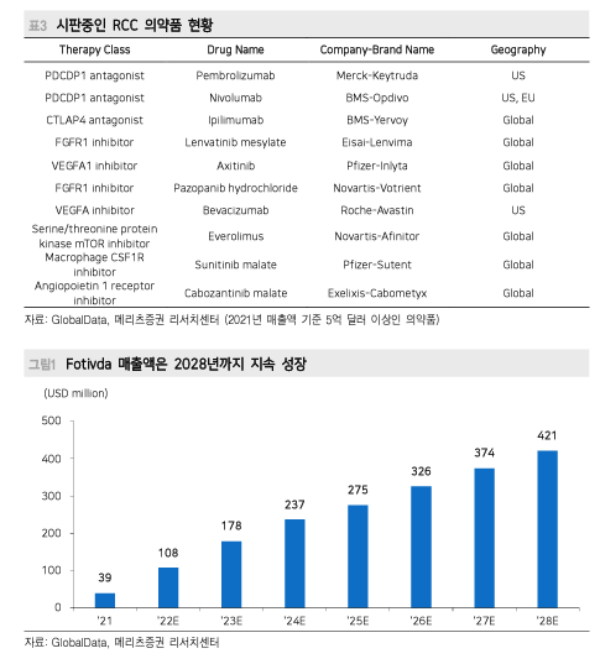
약 50%의 환자들이 재발 또는 불응성으로 진행해 2차 이상 치료제가 필요한 상황 TIVO-3(NCT02627963) 임상시험을 통해 이전에 2~3개의 systemic regimen에 실패한 성인 환자 350명을 대상으로 Fotivda(Tivozanib)와 Nexavar(Sorafenib)의 치료 효능을 비교평가 함.
각 군에 1:1로 무작위 배정되었고, 1차 평가변수는 Progression Free Survival(PFS, 무진행 생존기간)임. 2차 평가변수는 Overall Survival(OS, 전체 생존기간), Objective Response Rate(ORR, 객관적 반응률), Duration of Response(DoR, 반응 지속기간)임. Fotivda PFS 중앙값은 5.6개월, Nexavar는 3.9개월(HR 0.73; 95% CI: 0.56- 0.94; p=0.016)로 Fotivda의 PFS가 Nexavar 보다 유의미하게 김. 또한 ORR은 Fotivda 17.7%, Nexvar 8.0%를 기록.
이전에 면역항암제를 투여했었던 신세포암 환자에게 Opdivo(Nivolumab) 병용 3상 임상시험과 간암에서 Imfinzi(Durvalumab) 병용 2상 임상시험도 진행 중.
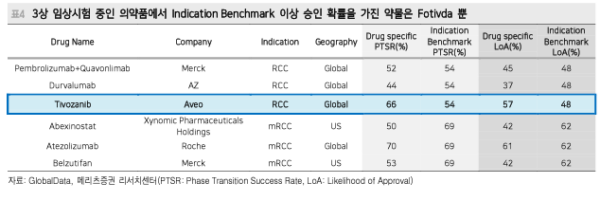
블록버스터 항암제들과 병용 임상시험 및 추가 적응증 확보를 통해 의약품의 적용 범위를 확장해 나갈 전망 GlobalData에 따르면 2022년 Fotivda의 예상 매출액은 약 1,539억원, 2028년 예상 매출액은 약 6,000억원 규모. LG화학 생명과학 사업부문의 매출액은 약 6,000억원에서 7,000억원 (LG화학 전체 매출액 대비 3%미만 수준).
신세포암 또는 전이성 신세포암을 대상으로 3상 임상시험 중인 약물 중에서 Indication Benchmark 대비 Drug specific PTSR(Phase Transition Success Rate)와 LoA(Likelihood of Approval) 값이 높은 것은 Fotivda가 유일.
향후 Fotivda의 적용 범위 확장을 통해 매출액 성장 예상 LG화학 생명과학 사업부문은 자체 개발 당뇨 신약 제미글로, 인간 성장호르몬제 유트로핀, 관절염주사제 시노비안 등을 시판 중. 이 밖에도 통풍 신약 티굴릭소스타트, NASH 치료제 등의 파이프라인을 보유.
당뇨, 백신, 의료기기 등 다양한 제품군을 확보하고 있지만 시판되는 항암제 제품군은 없음.
이번 인수를 통해 시판중인 항암제를 확보. 국산 신약 중 첫 미국 FDA 승인을 받은 팩티브의 노하우를 바탕으로 향후 미국 시장 진출에 교두보가 될 것으로 기대.
 |
 |
 |
<자료제공:메리츠증권>
박병우 기자 bwpark0918@pharmstock.co.kr
<저작권자 © 팜스탁, 무단 전재 및 재배포 금지>

 클리오, 일본 직접 한다
클리오, 일본 직접 한다




