�ʽ�Ź�� ������̿�������� ������ �߿� ���� ���� ��������ߴ�.<������ ��>
�����̿�������, �ڷγ� 19��� �߰� ���� �ӻ� 1/2�� IND ��û
�����̿��������� ��ǰ�Ǿ�ǰ����ó�� �ڷγ� 19 ���� ��� ���ڹ�-19 �߰����� 1/2�� �ӻ�����ȹ(IND)�� ��û�ߴٰ� 19�� �����ߴ�. ȸ������ "���ڹ�-19�� SARS-CoV-2 ������ �ܹ��� ������� ������ ������ �鿪�������� �����Ͽ� ���� ������ ����� COVID-19 ����ȿ���� ���ȴ�"�� "���庸���� ������ ������ �־� �߰����� �� ������� ���� ������ ���ȴ�"�� ������.
������̿�, �̱� �����Ͼƿ� '������̿� USA' �������� ����
������̿��� �̱� �������� �ڻ��� ���̷����� �ĺ������� CP-COV03�� ������� ��û�� �ļ� �ӻ� ������ ������ ��������� '������̿� USA'�� ���� 16��(�����ð�) �����Ͼ��ֿ� �����ߴٰ� 19�� ��ǥ�ߴ�. ������̿��� �ֱ� ���� �ֻ����� �ӻ��Ź���(CRO)�� �̱��� '����ť���'�� �ڹ������ ü���ѵ� �̾� �̱� ���α��� �ż��� ���������ν� CP-COV03�� ��� ������ ���� �մ���� �����̴�.
��Ʈ����, �ƹٽ�ƾ �ùз� '��������' ���� �Ǹ��㰡 ȹ��
��Ʈ������ ���� �Ǿ�ǰ �����籹���κ��� ���� '�ƹٽ�ƾ'(���и� ���ٽ��ָ�) ���̿��ùз��� '��������(CT-P16)' �Ǹ��㰡�� ȹ���ߴٰ� 19�� ������. ���� 8�� 18�� ����������������ȸ�κ��� �Ǹ��㰡�� ȹ���� �� �̾� �������� �߰��� �㰡�� ȹ���� ������ �ֿ���忡�� �Ǹ��㰡 ȹ���� �Ϸ��ߴ�.
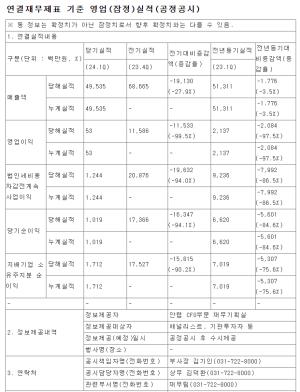
��������, ����ģȭ��å ��ȯ���� 20��� �Ը� �ڻ��� ���
�ڽ��� ������ ���������� ����ģȭ��å�� ��ȯ���� 20��� �Ը��� �ڻ��� ����� �����Ѵ�. �̹� �ڱ��ֽ� ����� �ڽ��� ���� �峻 �ż��� ����Ǹ�, ��� ���� ������ ������ 304,878��, ���ݾ��� 20������� 9�� 20�Ϻ��� 12�� 19�ϱ��� 3������ �����Ѵ�.
��������, ���ں� ��ġ����ȯ ġ���� ���� MOU
���������� ���� �žళ�� ������� (��)���ں� ��∙����ȭ ��ġ����ȯ ġ���� ���������� ���� ������ ��������(MOU)�� ü���ߴٰ� ������. �̹� �������� ���������� ��·����ȭ �ž� �ĺ������� ����ü �ռ�, ���� �� ����ǰ������(CMC) ������ �����ϰ� �Ǹ�, ���ں� �ڻ��� ���� �žళ�� �÷��� ‘TOFPOMICS(�������ͽ�)’�� ������� �ž� �ĺ����� ������ ���� �����ΰ� �ռ� ���� �ڹ� �� ������ �����ϰ� �ȴ�.
���ý�, 1�ִ� 100��→500�� �ֽĺ��� ����
���ý��� ������ 1�ִ� ������ 100������ 500������ �����ϱ�� �����ߴٰ� 19�� �����ߴ�. �ֽĺ����� ���� ���� �ֽļ� ������ ���� �ְ� ����ȭ �� �����ġ ������ ���� ������ �����ֽ� �Ѽ��� 34,223,815���� 6,844,763�ַ� ����ȴ�.
�ѿù��̿��ĸ�, ��ü�ž� HL161 �Ϻ� �ӻ� 3�� ����
�ڰ��鿪��ȯ ġ������ ���ߵǰ� �ִ� �ѿù��̿��ĸ��� ‘HL161(������: ����Ŭ����)’�� �Ϻ� �Ǿ�ǰ �� �Ƿ������û(PMDA, Pharmaceuticals and Medical Devices Agency)�κ��� �����ٹ����� �Ϻ� �ӻ� 3�� ������ ���� �Ҵ�. �ӻ� ��ȹ ���ο� ���� �ѿù��̿��ĸ�(���� �ѿ�)�� �̹³��Ʈ(Immunovant)�� ������ �� �Ϲݱ� ����Ŭ������ ȿ�ɰ� ������ ���� ���ϱ� ���� �ӻ� 3�� ������ �����̴�.
�Ŷ���, ������ �����κ��� ���� �ĺ����� ��� ����
�Ŷ����� ������ ������ �ٽǸ���(Basilea)�� ���� �ĺ����� ‘BAL0891’ ���� ����� ü���ߴٰ� 20�� �����ߴ�. �� ��� �Ը�� �� 3��3500�� ����, ������ 1400�� ��, ���ϵ彺���� �� 3��2100�� ����. ���ϵ彺���� ��κ��� ���ȭ�� ������ ��� �����ϴ� �����̴�.
�ø���, �� ����� Ȳ�ݺ���ġ���� 1�� ���Ͻ��� ����� ����
�ø����� ���� ���� �̳뺣�̼�(Théa Open Innovation, ���� ‘����’)�� ��������� �Ǽ� �� Ȳ�ݺ��� ġ���� ‘OLX301A’ ù ���Ͻ���(�ܰ躰 �����)�� �����ߴٰ� 20�� ������. ���� 7�� �ø����� �̱� (FDA�� OLX301A ��1�� �ӻ���� ��ȹ(IND)�� ������ �ӻ� 1�� �����Կ� ���� ���Ʒκ��� ��ȯ �ǹ� ���� ���Ͻ��� ����Ḧ ������ �����̶�� �����ߴ�.
���ٽÿ�, ����� 'EV����' �濵�� �μ�...������
�ڷγ����̷��� 99.9% ��Ȱ��ȭ �������� �� �������� '�ں��'�� ������ ���ٽÿ��� �ڽ��� ����� EV������ �濵���� �μ��ߴٰ� 20�� ������. ���ٽÿ��� EV���� �μ��� ��ȸ������ ���� �������� Ǯ�̵ȴ�.
�ij���, ���Ѿ���� ‘������’ �������� �������� ���� ����
���ij����� �������� ��������(Original CDx)�� ���� �����Ѵ�. �ij����� (��)���Ѿ���� ���Ѿ��� ��� ġ���� ‘������(���и� ������Ƽ��)’�� �ڻ� ��� ���� ��ǰ ‘�ij���Ÿ���� R EGFR’ �������� ��������(Original CDx) ���� ���� ����� 19�� ü���ߴ�.
��Ʈ����, 2�� 4,300��� �Ը� ������ü ���� ���� ���
��Ʈ���� ��Ʈ������ �̱� ���̿���ũ ���̺�����(Abpro)�� HER2 �缺 ������� ǥ������ �� ������ü ġ���� 'ABP102'�� ���������Ѵٰ� 20�� ������. �̹� ������� ��Ʈ������ ABP102�� �۷ι� ���� ���� �� �Ǹ� �Ǹ��� ������ Ȯ���ߴ�.
���������̿�, �ΰ��� 32�� ���� PCR ���� �ڷγ� �ڰ� ŰƮ ����
�۷ι� ü������ ��� ���������̿��� �ΰ����� ȹ�������� ����ø� ������ �ڷγ� �� �ڰ� ����ŰƮ ���߿� �����ϰ� �̱� Ư�� ����� ���ƴٰ� 21�� ������. �� ��ǰ�� CareSuperbTM COVID-19 Antigen Home Test��, ���� �̱� Ư��û������ Ư�� ����� �Ϸ������, �� ��������㰡(EUA)�� ���� �ӻ������ �� ������ ����� �����̴�.
���ڹ��̿���, �����̵�â ����ŰƮ �ľ�ó ���� �㰡
ü�������Ƿ��� ������ ���ڹ��̿��尡 ���� ���ʷ� �����̵�â PCR ����ŰƮ�� ��ǰ�Ǿ�ǰ����ó �����㰡�� ȹ���ߴٰ� 21�� ������. ���ڹ��̿��尡 �̹��� ȹ���� �����㰡�� ���� 2016�� ��������û�� �����뿪���� ������ ���� ������ �Ϸ��ϰ� ���� Ư�㸦 ����� �����̵�â ����ŰƮ�̴�.
�����̸ƽ�, "���ֹ��� �������� ������ …��ǹ���"
�����̸ƽ��� 22�� �ӻ��ڱ� ������ ���� ���ֹ��� �������ڸ� �����ϰ� �ִٴ� �ҹ��� ���� ����� �ƴ϶�� ������. �̿� ����, ȸ�� �����ڴ� "�¶��� Ŀ�´�Ƽ���� �ö���� ���ֹ��� �������� �������� �ٰ� ���� �ҹ�"�̶�� "�濵�� ���ο��� �������� ������"�� ���ߴ�.
���ǹ��̿�, ������̿� IPO���� ���� �� '���� ����'
����ĸ�� OEM/ODM ���� ������� �߾��ǹ��̿��� ���俹���� �̾� �Ϲݰ��� û����� ������ �ŵ״�. ���ǹ��̿��� 9�� 20�ϰ� 21�� ���ϰ� �Ϲ� û�� �ֽļ� 30�� �ֿ� ���� �Ϲ��� ��� ����û���� ������ ��� �Ϲ� û�� ������� 1518.2�� 1�� ����ƴ�.
������Ʈ, ڸ FDA �������̸Ӻ� ���ν��� �ӻ�1/2a�� ������û
������Ʈ�� �̱� FDA '�浵 �� �ߵ(mild to moderate) �������̸Ӻ� ȯ�ڸ� ������� �� ���ν���®�� ������ �� Ž���� ��ȿ���� ���ϴ� ��1/2a�� �ӻ�����ȹ��' �ӻú���(Inactivation)�� ��û�ߴٰ� 22�� �����ߴ�. ȸ������ "���ܰ� �ӻ��� ���� �ӻ�ٰ� ��Ȯ���� ���� ���� �ӻ��ȹ ���� �Ǵ� ���� ���� ���� �Ǵ��� �̷���� ������ �̱�FDA���� ���ι��� �ӻ����(IND)�� �ӻú��� (Inactivation) ��û�ߴ�"�� ������.
�̿��÷ο�, �½��� '�̿���ġ'�� �������� ��� ����
�̿��÷ο�� (��)�½��� �̿���ġ �� ������ǰ����� �����ߴٰ� 22�� �����ߴ�. ȸ������ "2017�� 09�� 05��(��������) �̿���ġ �� ADM�����ѹα��� �ǸŸ� ���Ͽ� ���������� (��)�½��� �����Ѵٴ� ����� ü���� �ٰ� �ִ�"�鼭 "���� �����Ǹ��� ��������� ���Ͽ� ��簡 �����Ͽ� ������ǰ�� ���Ͽ� �����ߴ�"�� ������.
�ѹ̾�ǰ, ڸ FDA "������Ƽ�� ������ ���躸�� ũ�� �ʴ�"
�ѹ̾�ǰ�� �̱� FDA �����ڹ�����ȸ(ODAC)���� 9:4�� ������Ƽ���� ������ ���躸�� ũ���ʴٰ� ǥ���ߴٰ� 23�� �����ߴ�. ȸ������ "�̱� FDA �����ڹ�����ȸ(Oncology Drug Advisory Committee)�� 2022�� 9�� 23��(���� �ѱ��ð�)�� ���ֵ� ��ûȸ���� ������Ƽ���� �ż��㰡�� ������ �ǰ��� ��ǥ�Ͽ���"�� "FDA�� ODAC �ǰ��� ������ ��� ��Ȳ�� ������ �� ó���Ǿ�ǰ ��û�� �������(Prescription Drug User Fee Act, PDUFA)�� ���� 2022�� 11�� 24�ϱ��� ������Ƽ�տ� ���� �����㰡 ���θ� ������ �����̴�"�� ������.
���ٴ�, ��2�� �索��ġ���� '����Ʈ����������' ǰ���㰡 ��û
���ٴ��� ��ǰ�Ǿ�ǰ����ó�� ����Ʈ����������(CKD-393) ���� ǰ���㰡�� ��û�ߴٰ� 23�� �����ߴ�. ����Ʈ������������ �κ��۸�Ÿ���� ��Ÿ�۸�ƾ �� ��Ʈ�������� ���������� ������ ���� ��2�� �索�� ȯ��ġ�����̴�.
��dz����, ���� ġ���� '�Ƕ�ƽ�' �۷ι� ���� �������� ���� ����
��dz�����ֽ�ȸ��� ���� ġ���� '�Ƕ�ƽ�'�� 269�� ��(��ȭ �� 36���) �Ը��� ������ ���� ���״�. �Ƕ�ƽ��� ù �۷ι� ���� �������� ���� �����̴�.
��������-�� UNITHER, ������ ��Ʈ�ʽ� ü��-�۷ι� ��� ����
����ȯ �Ǿ�ǰ ������� ��������(000520)�� �۷ι� �Ǿ�ǰ CDMO ��������� �������� UNITHER��� ������ ���� ������ ���� ��Ʈ�ʽ��� ü���ߴٰ� 23�� ������. ���� ������ ��Ʈ�ʽ��� ���� ���� 3�� ������ �������� �Ϲ̻繫���� �Ϲ̽��� ���� ������Ʈ�� ���� �Բ� ������ ���� ����ϰ�, ���������� �߽��� ������ ����� ��Ʈ�� ������ ����� �Բ� �ƽþ� ���������� CMO ��� ��ȸ�� �Բ� ����ϸ�, ����� ���� ������ ���� �پ��� ��ȣ ������ ����ߴ�.
���� ���� kimsarang0420
<���۱��� © �ʽ�Ź, ���� ���� �� ����� ����>

 EDGC, �������� ���� ��...�ֱǸŸ� �ŷ��Ⱓ�� ����
EDGC, �������� ���� ��...�ֱǸŸ� �ŷ��Ⱓ�� ����