팜스탁은 제약바이오종목들의 지난주 중요 동향등에 대해 요약정리했다.<편집자 주>
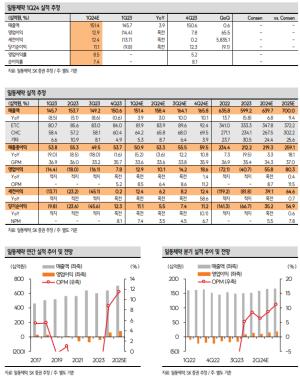
SK바이오팜, 663억원 규모 신약 세노바메이트 공급 계약 체결
SK바이오팜은 SK Life Science, Inc.와 663억원규모로 뇌전증 치료 신약 세노바메이트의 공급계약을 체결했다고 25일 공시했다. 공급금액은 최근 매출액의 15.9%에 해당되며 계약종료일은 10월31일까지다.
휴마시스, 코로나 자가검사키트 캐나다 인증-북미시장 공략
휴마시스가 당사의 자가검사키트에 대해 캐나다 개인용 인증(CE-Self testing)을 지난 22일(현지시간) 획득했다고 밝혔다. 이번 캐나다 승인을 기점으로 북미 시장에서 코로나 자가검사제품의 판매가 증가할 것으로 전망하고 있다.
크리스탈지노믹스, 제이앤씨사이언스 코로나 치료제 후보 발굴
크리스탈지노믹스와 제이앤씨사이언스는 화이자 팍스로비드와 동일 기전인 3CL프로테아제를 억제하는 코로나치료제 후보물질의 동물실험에서 안전성과 효능을 확인했다고 26일 밝혔다. JNC-11139는 소동물(마우스) 급성독성연구에서 하루 2000 mg/kg의 높은 농도에서 안전성을 확인했으며, 대동물(비글견)에서 경구 흡수율 68% 이상과 생체 내 반감기(약물농도 또는 양이 50% 감소하는데 걸리는 시간) 4시간 이상이 나타났다.
휴젤 보툴렉스, 미국 유럽 임상3상 결과 SCI급 국제학술지 게재
글로벌 토탈 메디컬 에스테틱 전문 기업 휴젤㈜은 자사의 보툴리눔 톡신 제제 ‘보툴렉스(수출명 : 레티보(Letybo))’의 미국·유럽 임상 3상 결과가 SCI급 국제 학술지인 ‘에스테틱 서저리 저널(Aesthetic Surgery Journal)’ 6월호에 게재됐다고 26일 밝혔다. 임상 3상은 미간주름 환자 1,200명 이상을 대상으로 무작위, 이중맹검, 위약대조 방식을 통해 약물의 유효성 및 안전성 등을 평가했는데, 이번 논문에서는 가장 최근 진행된 임상 결과가 발표됐다.
대웅제약, 탈모 치료제 ‘IVL3001’ 개발 순항
대웅제약이 인벤티지랩·위더스제약과 함께 개발 중인 탈모 치료 장기지속형 주사제 개발이 순항 중이다. 대웅제약은 지난 1년간 호주에서 진행한 탈모 치료 장기지속형 주사제 ‘IVL3001’(성분명: 피나스테리드)의 임상 1상 시험을 성공적으로 완료했다고 26일 밝혔다.
프레스티지바이오파마, 아바스틴 바이오시밀러 공급 계약
프레스티지바이오파마는 인도 인타스(Intas Pharmaceuticals Limited)와 아바스틴바이오시밀러 ' HD204'판매에 대한 라이선스·공급 계약을 체결했다고 26일 공시했다. 계약 판매지역은 미국을 비롯하여 유럽, 캐나다, MENA(Middle East North Africa), 브라질, 멕시코, 남아프리카, 태국, 베트남, 필리핀, 말레이시아, 싱가포르, 인도네시아, 키르기스스탄, 타지키스탄 등 총 82개국이며 라이선스 및 공급계약은 각 국가별로 제품 출시로부터 5년까지 유효하다.
올릭스, 노인성 황반변성 치료제 OLX301A 기술료 수령 예정
RNA 간섭 치료제 개발 전문 기업 올릭스가 떼아 오픈 이노베이션(Théa Open Innovation)에 기술이전한 건성 및 습성 황반변성 치료제(OLX301A)의 미국 임상 1상 진입 마일스톤 달성에 따라 1차 단계별 기술료를 수령할 예정이라고 26일 공시를 통해 밝혔다. 올릭스는 한국 시간으로 7월 1일 OLX301A의 임상시험계획서(IND)를 FDA에 제출해 ‘임상 1상 진입’이라는 마일스톤을 달성함에 따라 떼아에 마일스톤 기술료 인보이스를 발행했다.
큐라티스 결핵백신 ‘QTP101’, 글로벌 2b/3상 IND 승인
큐라티스는 지난 21일 식품의약품안전처로부터 QTP101 결핵백신 다국가 2b/3상 임상시험 IND(임상시험계획)를 승인받았다고 26일 밝혔다. 큐라티스는 국내 최초로 진행한 성인 대상 2a상 임상시험 및 청소년 대상 1상 임상시험에서 임상적으로 우수한 내약성과 안전성 프로파일을 확인했다.
한미약품, 노바티스 '엔트레스토' 후속 특허 4건 모두 승소
한미약품이 노바티스의 만성 심부전 치료제 ‘엔트레스토’의 용도특허 등 후속 특허 4건에 대한 도전에서 국내사 최초로 모두 승소하며 제품 출시를 위한 모든 준비를 마쳤다. 우선판매품목허가 요건까지 국내사 최초로 충족한 한미약품은 허가를 취득하는대로 후발 의약품을 출시한다는 계획이다.
현대바이오, 코로나 경구제 이름 '제프티(Xafty)'로 확정
현대바이오사이언스는 니클로사마이드를 주성분으로 한 자사의 코로나19용 먹는 항바이러스제 후보물질(CP-COV03)의 약물이름(브랜드)을 '제프티(Xafty)'로 확정했다고 27일 발표했다. 제프티는 '빠른 치료'를 뜻하는 'Fast treatment', '안전을 떠오르게 한다'는 의미의 'evoke safety'의 합성어로, 고대 이집트 신화에 등장하는 지식과 과학의 신 '제후티'(그리스 이름 토트, Thoth)에서 따왔다고 현대바이오는 설명했다.
삼성바이오로직스, 올해 매출 2조원 클럽 가입 확실
삼성바이오로직스가 올해 연간 매출 2조 원 돌파도 무난할 것으로 분석됐다. 연결기준 상반기 매출은 1조1,627억, 영업이익 3,461억원으로 자회사 삼성바이오에피스(이하 에피스) 실적을 제외한 삼성바이오로직스 개별 기준 상반기 매출도 1조를 넘어선 1조150억원으로 집계됐다.
앱클론, 유펜 의대와 CAR-T 치료제 공동연구 확대
앱클론이 펜실베니아 대학교(University of Pennsylvania, U-Penn) 의과대학 세포면역치료제센터 마르코 루엘라 교수팀과 카티(CAR-T) 치료제 개발에 대한 공동연구를 확대키로 하는 계약을 체결했다고 28일 밝혔다. 펜실베이니아 대학교 의과대학은 카티 치료제 선도적 연구 명성을 갖고 있는 대학으로, 이를 노바티스에 기술이전(L/O)해 2017년 기적의 항암제로 불리는 세계 최초 카티 치료제 제품 ‘킴리아’를 탄생시킨 것으로도 잘 알려져 있다.
제일약품, 日시오노기 항생제 국내 독점 계약 체결
제일약품은 핑안 시오노기(Ping An-Shionogi, 대표 타츠모리 요시다)와 사이드로포어 세팔로스포린(Siderophore Cephalosporin) 항생제 성분인 ‘세피데로콜(Cefiderocol)’에 대한 국내 독점 공급 계약을 체결했다고 28일 밝혔다. 핑안 시오노기는 일본 시오노기社와 홍콩 핑안社와의 합작 법인으로 원개발사인 시오노기로부터 ‘세피데로콜’의 아시아 판권을 보유하고 있다.
툴젠-제농S&T, 고부가가치 기능성 종자개발 업무협약 체결
㈜툴젠과 ㈜제농S&T 농업회사법인(대표이사 김태형)은 유전자교정 기술을 이용해 새로운 품종개발 연구협력을 하고자 상호업무협약을 27일 체결했다. 제농S&T는 1968년 설립돼 고품질, 내병계 채소종자 개발과 양파 및 수박, 무 등 신품종을 육성해 국내 보급 및 해외수출을 확대하고 있는 농업회사법인이다.
HLB생명과학, 천연물 유래 의약품 소재 개발 위한 MOU 체결
HLB생명과학(067630)은 한국과학기술연구원(KIST) 강릉 천연물연구소와 ‘천연물 유래 조성물 공동 연구개발 상호 양해각서(MOU)’를 체결했다고 28일 밝혔다. HLB생명과학은 이번 협약을 통해 천연물 유래 항암 신약과 건강기능식품, 화장품 소재 등을 연구할 방침이다.
SK바이오사이언스,코로나19 백신 '스카이코비온' 英 허가 신청
SK바이오사이언스 '스카이코비온'(GBP510)에 대해 영국 의약품 규제당국인 MHRA(Medicines and Healthcare product Regulatory Agency)에 '18세 이상 성인에서 SARS-CoV-2 감염에 의한 COVID-19 질병 예방'을 적응증으로 조건부허가(CMA)를 신청했다고 29일 공시했다. 스카이코비원은 이미 지난 3월부터 MHRA에서 신속 승인을 위한 순차심사(Rolling Review)를 진행 중으로, 최근 확보한 임상 3상 데이터 등을 포함해 정식 조건부 허가 심사 신청을 통해 본격적인 품목 허가 심사에 돌입하게 된다.
압타바이오, 당뇨병치료제 APX-115 임상 2상서 유효성 입증
압타바이오가 아이수지낙시브(Isuzinaxib, APX-115) 당뇨병성 신증 치료제 임상 2상에서 통계적 유효성을 입증했다고 29일 임상 2상 결과 공시를 통해 밝혔다. 이번 압타바이오가 임상2상 결과를 발표한 당뇨병성 신증은 현재 전 세계적으로 허가받은 치료약은 없으며 질환 발생 시 고혈압 치료제인 ACE inhibitors 또는 ARB가 처방되고 있다.
동아ST, 당뇨병 복합제 ‘슈가다파정’ 품목허가 신청
동아에스티는 식품의약품안전처에 제2형 당뇨병 복합제 ‘슈가다파정’의 품목허가를 신청했다고 29일 밝혔다. 슈가다파정은 동아에스티가 개발한 DPP-4 억제제 당뇨병 신약 ‘슈가논’의 주성분인 에보글립틴(Evogliptin) 5mg과 SGLT-2 억제제 계열의 다파글리플로진(Dapagliflozin) 10mg을 결합한 복합제다.
김사랑 기자 kimsarang0420
<저작권자 © 팜스탁, 무단 전재 및 재배포 금지>

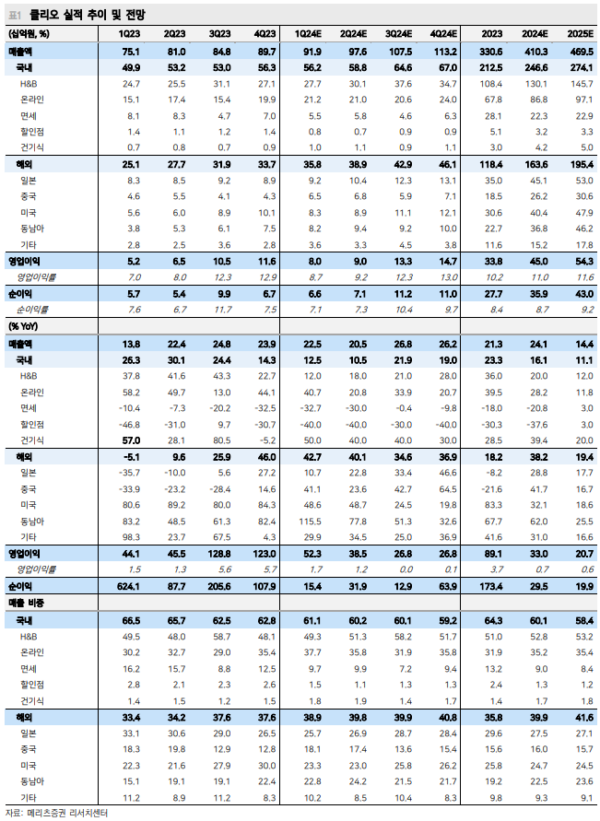 클리오, 일본 직접 한다
클리오, 일본 직접 한다