셀트리온의 COVID19 항체치료제 임상 2상 결과
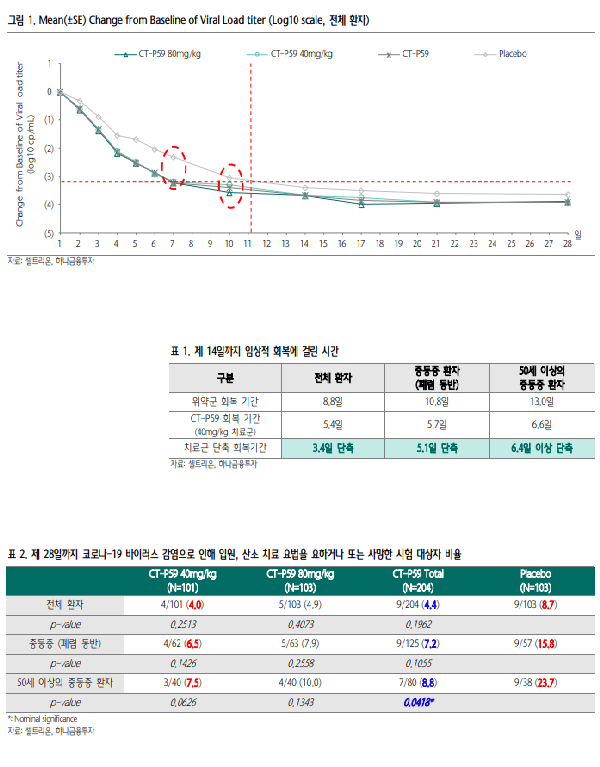
1월 13일 셀트리온은 ‘2021 하이원 신약개발 심포지아’에서 COVID19 항체치료제인 렉키로나주(성분명, Regdanvimab, 개발명, CT-P59)의 글로벌 임상 2상 결과를 발표했다. 총 307명 환자의 임상결과로, 모집된 환자는 경증 및 중증도의 외래환자로 구성되었으며, 이중 60%는 폐렴을 동반한 중등증 환자였다. 임상결과 1) 경증 및 중등증 환자가 입원치료를 필 요로 하는 중증으로 발전하는 발생률은 투약군(40mg/kg)에서 위약군 대비 전체 환자의 경우 54%, 50세 이상 중등증 환자군 의 경우 68% 감소시켰다. 2) 임상적 회복기간은 전체 환자대 상 3.4일 이상 단축(8.8일→5.4일), 폐렴을 동반한 중등증 환 자의 경우 5.1일, 50세 이상 폐렴을 동반한 중등증 환자의 경 우 무려 6.4일 이상 단축되는 효과를 보여주었다. 3) 또한 렉 키로나주 투약군에서 체내 바이러스의 농도가 위약군 대비 7일 째 기준 현저하게 낮게 나타났다. 안전성 평가 결과, 중대한 이상반응이나 사망 발생 사례는 나타나지 않아 우수한 안전성 을 입증하였다.
리제네론과 일라이릴리 항체치료제의 사례
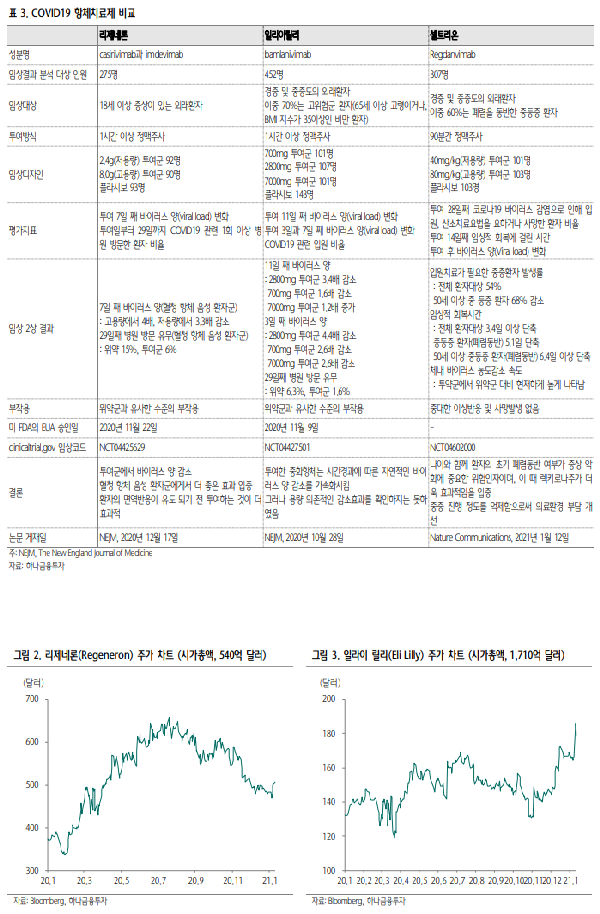
미국에서는 2020년 11월 9일과 11월 22일 일라이릴리사의 bamlanivimab과 리제네론의 REGN-COV2(casirivimab과 imdevimab의 칵테일)가 각각 미 FDA로부터 긴급사용허가 (EUA) 승인을 획득하였다. 셀트리온의 렉키로나주와 동등한 조건 및 임상평가지표로 직접 비교한 임상결과는 없기에 세 종 류의 항체치료제 중 어떤 제품이 더 우월하다라고 단정적으로 언급하기는 어렵다. 그러나 주요 객관적 지표라고 할 수 있는 투약 후 체내 바이러스 양(Viral load)의 감소효과 추세가 비슷 하게 나왔다는 점에서 기존 EUA 승인을 획득한 항체치료제와 비교할 만하다고 할 수 있다. 일라이릴리의 경우 바이러스 양 감소효과가 농도의존적으로 나타나지 않았기에 셀트리온의 임 상결과가 더욱 의미있다고 할 수 있다. 특히 투약 후 7일째, 베이스라인 대비 바이러스 양의 변화값이, 구체적인 숫자가 발 표되지 않았지만, 위약군 대비 투약군에서 약 -0.9 이상 발생 했다면 바이러스 양이 약 8배 이상 감소했다고 볼 수 있다.
렉키로나주의 개발 의의와 한계
이번 셀트리온이 발표한 COVID19 항체치료제는 셀트리온이 자체 개발한 신약이다. 기존 바이오시밀러 개발사라는 한계를 넘어 셀트리온이 신약개발 역량도 충분히 있음을 이번 임상결 과 발표로 보여주었다고 할 수 있다. 그러나 렉키로나주로 인 한 셀트리온의 실적 개선효과를 기대하기에는 한계가 존재한 다. 12월 29일 국내 식약처에 조건부 허가 신청서를 제출, 2월 초 조건부 허가 승인을 기대할 수는 있으나, COVID19 환자 수가 적고 시장규모도 작은 국내에서의 시판이 실적 개선효과 로 이어지기는 어려울 것으로 보인다. 향후 당연히 미국이나 유럽시장에 진출할 것으로 예상되지만, 임상결과 효과가 좋았 던 리제네론의 항체치료제도 현지 미국 병원에서 처방되는 비 율은 20%에 불과, 항체치료제가 COVID19 치료제의 게임체인 저가 되기는 어렵다는 분석이 지배적이다. COVID19 치료제에 대한 좀 더 냉철한 판단이 필요한 시점이다. <자료제공:하나금융투자>
 |
 |
김사랑 기자 kimsarang0420
<저작권자 © 팜스탁, 무단 전재 및 재배포 금지>

 씨엔알리서치-로피바이오, FDA 아일리아 임상 3상 IND 승인
씨엔알리서치-로피바이오, FDA 아일리아 임상 3상 IND 승인




