팜스탁은 제약바이오종목들의 지난주 중요 동향등에 대해 요약정리했다.<편집자 주>
유한양행-앱클론, 코로나19 항체치료제 공동 개발
유한양행은 5월부터 앱클론과 코로나19 항체치료제 공동개발을 시작했다고 밝혔다. 회사 측에 따르면 항체 기반 치료제 전문기업인 앱클론은 올해 2월부터 코로나19 항체치료제 발굴에 착수해 사람의 ACE2단백질과 바이러스의 스파이크 단백질 간 결합을 차단하는 초기 항체 후보물질 20종을 발굴했고, 최적화 과정을 통해 최종 항체신약 후보를 도출하는데 성공했다.
대웅제약-지노믹트리, 코로나19 진단키트 해외공급 계약 체결
대웅제약은 지노믹트리와 신종 코로나바이러스 감염증(코로나19) 분자진단 키트인 아큐라디텍(AccuraDtect SARS-COV-2 RT-qPCR Kit)의 글로벌 판매 및 공급 계약을 맺고 공동 협력에 나선다. 대웅제약에 따르면 아큐라디텍(AccuraDtect)은 코로나19 바이러스 감염 시, 일반적으로 검출하는 N2 유전자 외에 감염 세포 내 가장 많이 존재하는 리더 서열(Leader sequence)을 타깃 해 바이러스 감염 여부를 진단한다. 유전자 증폭기술인 실시간 중합효소연쇄반응법(RT-qPCR)으로 바이러스 유전자를 폭발적으로 늘려 검출하기 때문에 정확도(민감도, 특이도)가 높고, 검체 채취 후 4시간 이내에 결과 확인이 가능한 고감도 코로나19 분자진단 키트다.
엑세스바이오, 코로나19 진단키트 美 FDA 긴급사용승인
우리들제약이 최대주주인 엑세스바이오의 코로나 항체 신속진단키트가 미국 FDA로부터 지난 26일 긴급사용승인(이하 EUA)을 획득했다고 밝혔다. 회사 관계자는 "외부기관에서의 성능 평가 등 미 FDA의 변경된 제도에 부합하는 기준을 충족시키기 위해 예상했던 것보다 많은 시간이 소요됐다. 그러나 강화된 제도로 인해 IgG와 IgM을 구별해 동시에 진단하는 항체 진단키트중, 현재 EUA 허가 제품을 보유하고 있는 업체는 당사를 포함 단 10곳에 불과하다”고 전했다.
아라바이오, 치매치료제 'AR1001' 국제AAIC서 연구결과 공개
아리바이오는 개발중인 치매 치료제 AR1001의 다중기전 연구 결과를 알츠하이머협회 국제컨퍼런스에서 최초로 공개한다. 이번 학회에서 발표되는 연구 내용은 국내 바이오 벤쳐가 다중기전 전략을 통해 치매 치료제 개발의 새로운 패러다임을 제시하는데 큰 의미가 있다.
수젠텍, 코로나19 항체 진단키트 美 FDA 긴급승인 임박
수젠텍의 코로나19 항체 신속진단키트 'SGTi-flex IgM/IgG'가 최근 미국 FDA의 긴급사용승인 (EUA)을 받기 위한 성능평가에서 높은 민감도(양성을 양성으로 판별하는 능력)와 특이도(음성을 음성으로 판별하는 능력)를 최종 입증했다. 수젠텍은 미국 NCI(National Cancer Institute)에서 진행한 성능평가에서는 민감도 100%(임상샘플 30개), 미국 임상시험기관에서는 특이도 99%(임상샘플 121개)로 높은 정확도를 나타냈다고 28일 밝혔다. 이번 결과는 한국에서 진행한 임상시험 결과인 민감도 94%(임상샘플 163개), 특이도 98%(임상샘플 360개) 보다 높은 수치다.
동화약품, 척추 임플란트1위 기업 메디쎄이 인수
동화약품은 (주)메디쎄이를 인수한다고 밝혔다. 동화약품은 메디쎄이 인수를 통해 의료기기 사업 영역에 진출한다. 이번 인수는 최근 AI 헬스케어 솔류션 기업 뷰노 지분 투자 등 전통 제약산업 외 신규 헬스케어 사업영역에 본격적으로 진출한다는 점에서 의미가 있다고 회사 측은 설명했다.
한독 국내판매 '글라지아' 바이오시밀러신약 美 FDA승인
한독이 국내 판매하고 있는 ‘글라지아 프리필드펜(성분명: 인슐린 글라진, 이하 글라지아)’이 6월 11일 미국 식품의약국(FDA)으로부터 기저 인슐린 바이오시밀러 신약(미국 제품명: 셈글리(Semglee)으로 승인 받았다, 글라지아는 하루 한 번 투여하는 기저 인슐린으로 오리지널 의약품인 ‘란투스’ 바이오시밀러다. 인도 제약사 바이오콘이 개발했으며 GC녹십자가 국내 판권을 보유하고 한독이 2018년 11월부터 국내 판매 및 마케팅을 담당하고 있다.
티움바이오, 자궁내막증 치료제TU2670 유럽 임상 2a상
희귀난치성질환 치료제 연구개발 전문기업인 티움바이오가 자궁내막증 신약후보물질 TU2670의 유럽 임상 2a상 승인 계획을 러시아연방 보건부 MOH(Ministry of Health of Russian Federation)에 신청했다. 티움바이오는 TU2670 임상 2a상을 통해 80명의 자궁내막증 여성 환자들을 대상으로 유럽 내 5개국 총 40개의 임상시험기관(우크라이나 5개 기관, 러시아 6개 기관)에서 자궁내막증에 대한 약효를 검증하기 위하여 TU2670 반복 경구 투여에 대한 안전성, 약동학, 약력학을 확인할 예정이다.
한미약품, 포지오티닙 2상 긍정적.. 美 FDA 신약허가 추친
한미약품 파트너사 스펙트럼은 ‘포지오티닙’ 글로벌 2상(ZENITH20)의 두 번째 코호트 연구 결과를 28일 발표했다. 스펙트럼은 이번 연구 결과를 토대로 NDA(신약허가신청) 계획 논의를 위한 미국 식품의약국(FDA)과의 미팅을 추진할 계획이다. 한미약품이 개발해 지난 2015년 스펙트럼에 라이선스 아웃한 포지오티닙은 현재 Exon20 변이 폐암 및 유방암 등의 치료를 위한 혁신신약으로 개발되고 있다.
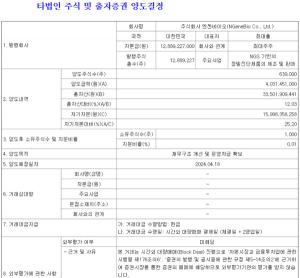
영진약품, 중국제약사와 210억원규모 원료의약품 계약
영진약품은 중국 GUANGSHOU TOSUN PHARMACEUTICAL.,LTD와 210억원 규모의 Cefcapene Pivoxil(원료) 공급 계약을 체결했다고 28일자로 공시했다. 계약금액은 최근매출액대비 9.5%에 해당하는 금액이다.
엑세스바이오, 코로나19 항체 신속진단키트 브라질 등록
우리들제약이 최대주주인 엑세스바이오는 최근 미국 FDA승인을 받은 코로나 항체 신속진단키트가 브라질 식약위생감시국(ANVISA)로부터 긴급사용을 위한 제품 등록을 완료했다. ANVISA로부터 승인받은 CareStart COVID-19 IgM/IgG는 최근 미 FDA의 EUA 승인을 받은 동일한 제품으로, 미국 국립암연구소로부터 민감도 100%, 특이도 97.5%를 입증받았다.
GC녹십자, 코로나19 혈장치료제 임상 2상 IND 신청
GC녹십자는 코로나19 혈장치료제 ‘GC5131A’의 임상 2상 IND(임상시험계획서)를 식품의약품안전처에 신청했다고 29일 밝혔다. 이번 임상시험의 목적은 약물의 적정 용량을 설정하고, 안전성과 유효성을 탐색하는 것이다.
셀트리온,코로나19 항체치료제 영국 임상1상 승인
셀트리온은 코로나19(코로나바이러스감염증-19, COVID-19) 항체 치료제CT-P59 임상시험계획(IND)을 영국 의약품건강관리제품규제청(MHRA)으로부터 29일(현지시간) 승인 받고 현지에서 환자 모집에 본격 돌입한다고 30일 밝혔다. 이번 영국 임상 1상은 코로나19 경증환자 대상으로 CT-P59의 바이러스 중화 효능과 약효 등 약물 유효성 초기 지표를 확인하는 것에 중점을 둘 예정이다.
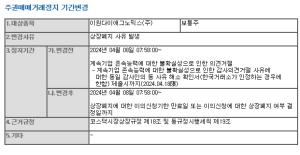
임시공휴일(8월 17일), 증권∙파생∙일반상품시장 휴장
한국거래소는 8월 17일 정부의 임시공휴일 지정에 따라 증권·파생·일반상품시장을 휴장한다고 밝혔다. 대상시장은 증권시장(주식시장, 증권상품시장(ETF, ETN, ELW), 수익증권시장, 신주인수권증서·증권시장, 채권시장(Repo포함) 및 KSM(KRX Startup Market))과 파생상품시장(CME 및 EUREX 연계 글로벌시장 포함) 및 장외파생상품(원화IRS, 달러IRS) 청산업무와 일반상품시장(석유, 금, 배출권)이다.
동아에스티,810억투입 송도공장 신설-글로벌시장 확대
동아에스티는 810억원을 투입하여 인천 송도공장을 신설한다고 30일자로 공시했다. 송도신공장은 고형제 국내 매출 증가와 향후 해외 판매 확대를 위한 기반 조성하기 위한 것이라고 밝혔다.
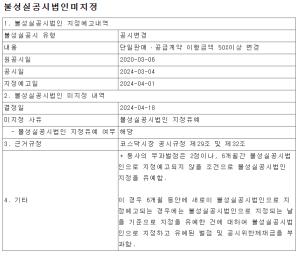
한국파마, 청약경쟁률 2035.74:1-8월 10일 코드닥 상장
한국파마가 29~30일 일반투자자 대상으로 공모 청약을 진행한 결과 2035.74:1의 청약 경쟁률을 기록했다고 30일 밝혔다. 한국파마는 지난 22일~23일 기관투자자를 대상으로 진행한 수요예측 결과, 경쟁률 1,296.86:1을 기록하며 공모가가 희망공모가 범위(6,500원~8,500원)의 상단을 초과한 9,000원으로 최종 확정됐다.
휴온스, ‘랄록시펜’ 코로나19 치료제 개발 착수
㈜휴온스는 지난 30일 본사에서 ‘신종 코로나 및 바이러스 억제 효과가 확인된 랄록시펜 및 신물질 10종에 대한 기술이전 및 공동연구개발 계약’을 체결했다. 앞서 휴온스는 경기도경제과학진흥원이 주관한 ‘신종 코로나 항바이러스 물질 및 용도특허 기술이전 대상기업 공모’에 우선협상대상자로 선정됐으며, 이번 본계약 체결로 이어졌다.
셀리드, 코비드-19 예방 백신 개발 국책과제에 선정
셀리드는 아데노바이러스 벡터에 기반한 1세대 및 2세대 코비드-19 예방백신 개발이 국책과제에 선정됐다고 31일자로 공시했다. 회사측은 "코비드-19 예방백신을 개발함으로써 국민의 불편함을 해소하고 정상적인 사회활동을 통한 국민생활 정상화에 기여하하겠다"며 "이를 통해 위축된 국가경제 및 산업 활성화에 기여할 것"이라고 밝혔다.
김사랑 기자 kimsarang0420
<저작권자 © 팜스탁, 무단 전재 및 재배포 금지>

 씨엔알리서치-로피바이오, FDA 아일리아 임상 3상 IND 승인
씨엔알리서치-로피바이오, FDA 아일리아 임상 3상 IND 승인