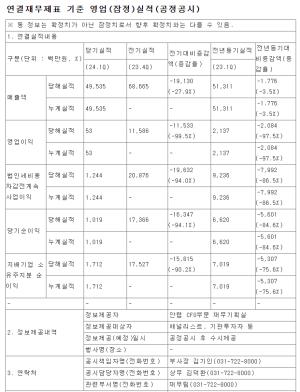
�ʽ�Ź�� ������̿�������� ������ �߿� ���� ���� ��������ߴ�.<������ ��>
��Ʈ����, ���ø�SC �����Ǿ�ǰû�� �ǸŽ��� �ǰ�(9/23)
��Ʈ������ 23��(�����ð� ����) �����Ǿ�ǰû(EMA) ���� �����ڹ�����ȸ(CHMP)�κ��� ���� ���� ���ø��ø�(Infliximab) �����ֻ� ���� '���ø�SC'�� ���� '�Ǹ� ���� �ǰ�' �ǰ��� �Ҵٰ� ������. '���ø�SC'�� '���ø�'�� ���� �����ֻ�(IV)���� �����ֻ�(SC)�� ������ ������ ��ü �����ѹ��̿��Ǿ�ǰ����, EMA������ ���� �������� ‘���̿�����(Biobetter)’ ������ Ȯ�� ��û (Extension Application)�̶�� ���� ���̿��ùз��� ����ȭ�� ���� ������ ��� �Դ�.
�ڿ��ջ�������, ڸ FDA '�κ���' �߰� �ڷ� ���� �䱸(9/23)
�ڿ��ջ��������� �ڿ���Ƽ������ ���� 20�� �̱� ��ǰ�Ǿ౹(FDA)���κ��� ������� ����������ġ���� �κ����� �̱� �ӻ�3��� ������ �ӻ��ߴ� ����(Continue Clinical Hold) ������ �����ߴٰ� 23�� �����ߴ�. �ڿ���Ƽ������ 2019�� 5�� 3��(�ѱ� �ð�) Clinical Hold �������� �䱸�ϰ� �ִ� �ڷ���� 2019�� 8�� 23��(�̱� �ð�) �̱� FDA�� �����Ͽ����� �̹� Continue Clinical Hold ������ �̿� ���� ȸ���̸�, �߰� �ڷ� ������ �䱸�ϴ� ���̶�� ������.
���ƿ���Ƽ, ���̿��ùз� ‘DA-3880’ �� �����Ǹ� ����(9/23)
���ƿ���Ƽ�� �Ϻ� ��Ʈ�ʻ��� ��ȭȭ�п�����(Sanwa Kagaku Kenkyusho, SKK, ��ǥ�̻� ���� ��Ÿ ī����)�� ������ �����������ڱ����� �ٺ�����ƾ-����(Darbepoetin-α) ���̿��ùз� ‘DA-3880’�� �Ϻ� �� �����Ǹ� ������ �Ļ��뵿�����κ��� ȹ���ߴٰ� 23�� ������. �ռ� 2014�� 1�� ���ƿ���Ƽ�� SKK�� DA-3880�� �Ϻ� �� ���� �� �Ǹſ� ���� ���̼��� �ƿ� ����� ü��������, SKK�� 2015�� �ӻ�1���� �������� �Ϻ� �� ������ ������ �Դ�.
�������̿�, �� ��ȥ������ 6,000�� �Ը� ‘�� ��� �ž�’ ����(9/23)
����Ƿ� ���� ��� �������̿��� 9�� 18�� �Ϻ� ��� �����(����������, Nippon Zoki Pharmaceutical, ���� ��ȥ������)�� 6,000�� ��(��ȭ �� 5�� ��) �Ը��� ������ž� ‘�뺸�ý� ��Ƽ’(NOVOSIS PUTTY) ���� ����� ü���ߴ�. ��� �Ⱓ�� 15���̸�, ������ 1,200�� ��(��ȭ �� 143���)��. �������̿��� ��ȥ�����翡 �����ϰ� �� �뺸�ý� ��Ƽ�� ���� 2009��-2014�� ���İ�����(�� �������ڿ���) �����õ������� ����� ���� 30����� R&D �ڱ� ������ �� ���ߵ� ��ǰ�̴�.
�︯���̽�, �����ý�(VM202) �ӻ� 3�� ��� ���� ����(9/24)
�︯���̽��� �索�����Ű溴��ġ���� �����ý�(VM2020)�� �ӻ� 3�� ��� ��� �����ߴ�. �︯���̽��� �索���� �Ű溴�� ġ���� VM202�� 3�� ����� � ȥ�� ���ɼ��� �߰ߵƴٸ� �̿� ���� ����� ȥ�� ���ɼ����� �ö�ú��� �����ý�(VM202)�� ȿ���� ũ�� �ְ�� ��Ȯ�� (��ȿ���� ����) ��� ������ �Ұ����ϰ� �ƴٰ� 23���ڷ� �����ߴ�.
���ٴ�, ����ġ�� ���̿��ùз� '����' �Ϻ� �㰡(9/24)
���ٴ��� �Ϻ� �Ļ��뵿�����κ��� ���� ���� 2���� ����ġ���� ���̿��ùз� ‘����’�� �Ϻ� �� �����Ǹ� ������ ȹ���ߴٰ� 24�� ������. ���ٴ��� ������ 4�� �̱� �۷ι� ����ȸ�� ‘���϶�(Mylan N.V.)’�� �Ϻ����ΰ� ������ �Ϻ� �� �㰡�� ���� �ӻ���� ����� ��ǰ�㰡, ��ǰ ���� �Ǹſ� ���� ����� ü�������� 10�� �Ļ��뵿���� �����Ǹ� ������ ��û�� �� �ִ�. ���ٴ��� ������ ����ǰ�� ���϶� �Ϻ����ο� �����ϰ� ���϶� �Ϻ������� �డ ���� ������ ���� 12�� �� ��ǰ�� ���, �Ϻ� �ǸŸ� �ð� �ȴ�.
���̿��ַ��, īƼ������ �ӻ� 3�� ���� ��ȹ ����(9/25)
���̿��ַ���� �ľ�ó�� ���� īƼ������(�ټ��ڰ���������������)�� �ӻ�3�� ���� ��ȹ ���ιҴٰ� 25���ڷ� �����ߴ�. ȸ������ "���� ���������� ����� �ִ� ����� (���豺 52�� ������ 52��)�� ������� �ڰ����� ������ġ����(īƼ������)�̽İ� �̼�õ���� ���� ġ�� ȿ���� MRI(MOCART total score) �� KOOS(Knee injury and Osteoarthritis Outcome Score)�� �� ���ϱ� ���� ��"�̶�� ������.
��ص��ĸ���,����ȭġ���� �̱� FDA ����Ǿ�ǰ ����(9/25)
�������̿������� ������ ���̿���ó ��ص��ĸ����� �����ϴ� �ž��� �̱� ����Ǿ�ǰ�� �����ƴ�. ���༺ ���Ű���ȯ �ž� ���߾�ü ��ص��ĸ��� ��ȸ�� ���������̺�νý��� ���� �������� ����ȭ ġ���� ‘TLY012’�� �̱� FDA�κ��� �������忰�� ���� ����Ǿ�ǰ���� �����ƴٰ� 25�� ������.
����ġ����, ڸ FDA ��������� Pre-NDA�ڷ� ���� �Ϸ�(9/25)
����ġ����� �̱� FDA�� 10��24�� ������ ��ȸ�� �������� '���������' �ž��㰡 ��������(Pre-NDA Meeting)�� ������ �ڷ������� �Ϸ��ߴٰ� 25�� ������. ������ Alex Kim ��ǥ�� “ ��������� �۷ι� �ӻ�3�� ���迡 ������ �ٽ� ��������� �̱� �ں����� FDA ��� ��������� ������ TFT���� ���� ��ǥ�� �ž��㰡��û(NDA) ���� ���ɼ��� �ش�ȭ�ϱ� ���� �ڷ� ������ ���� �������� ���ð���� ���� ��� �غ� ���ƴ�”�� “ FDA�ǹ��ڵ�� ���ǿ��� ��ǥ�� ������ �����ϱ� ���� ���� �Ⱓ ���ȿ��� ������ ���� ��”�̶�� ������.
����, ������ '�����ڰ���' Ư����� �ŵ�(9/26)
�������� ������б��� 25�� ����뿡�� '�����ڱ��� �Ż�� â��'�� ���� �ٰ��� ������ ������ ���� MOU�� ü���ߴ�. ������ ������ ������б��� �̹� ���¹�� ��ǥ�� 2018�� ����� ũ������ �����ڰ��� Ư��� ���õ� ��ġ�� �� �߸��� ���� �̽��� ���� ����� ���ǿ� ������ ���̴�. �� ���ư� �����ڱ��� �о߿��� ����� ���°��踦 ������ �������� �Ż�� �о� �̷� ���嵿���� �Բ� â���Ͽ� ���� ���б�� ������ �̹������� ��ǥ�� �ϰ� �ִ�.
�ľ�ó, ���Ƽ�� ����� 269ǰ�� ���� �Ǹ� ����(9/26)
��ǰ�Ǿ�ǰ����ó�� ���˾�ġ������ ������ �ĵ��� ġ������ �ֿ���� ���Ǵ� ���� ���� ‘���Ƽ�� ���� �����Ǿ�ǰ’�� ����·�˻��� ���, NDMA�� �������������� �ʰ��Ͽ� ����Ǿ��ٰ� ������. �̿� ���� �ľ�ó�� ‘���Ƽ�� ���� �����Ǿ�ǰ’�� ����� ���� ���� �����Ǿ�ǰ ��ü(269ǰ��)�� ���� ���������� ����·���� �� �ǸŸ� �����ϰ�, ó���� �����ϵ��� ��ġ�ߴ�.
JW�߿�����, �� �ɽþ ��dz�� 7õ���� ��� ����(9/27)
JW�߿������� �߱� �ɽþ� �ĸ���Ƽ�� ���� �迭���� ��¡ �ɽþ� ������ �ĸ���Ƽ�ð� ��dz ġ���� 'URC102'�� ���� ���̼��� �ƿ� ����� ü���ߴٰ� 27�� �����ߴ�. JW�߿������� �� ���� �ɽþ�κ��� Ȯ���� ���� 500�� ��(�� 60���)�� �ӻ�, �㰡, ���ȭ, �Ǹ� �� �ܰ躰 ���Ͻ������� �ִ� 6500�� ��(�� 781���)�� ���������� �ް� �ȴ�. ��ǰ ��� ���Ŀ��� �ɽþ��� �� ����� ���� �� �ڸ��� ������ �ο�Ƽ�� �´�.
GC���������, ���� 1��1300�� Ȯ��..��� �ֻ��(9/27)
���� ������ �コ�ɾ� �ַ�� ���� ��� GC��������� �� ���� 24�ϰ� 25�� ������ ��������ڸ� ������� ������ ���俹�� ���, ���𰡸� ��� �ֻ���� 11,300������ ���� Ȯ���ߴٰ� 27�� ������. �̿� ���� ����ݾ��� 509������� ���� Ȯ��������, ���� �� �ð��Ѿ��� ���� ���� 2,008��� �����̴�. �̹� ���俹������ ������ 1,071�� ����� ������ 19�� 244���ָ� ��û, �ܼ������ 657.93 �� 1�� ����ߴ�.
���̹��� �ֿ����
��9��30
-�ڿ��ջ�������, �Ҽ��ǰ��ù�������(�Ҽ� ���� �������û' ���ú�����)
��10�� 1��
-����Ʈ���� �����պ�(����Ʈ�������̿�)
���� ���� kimsarang0420
<���۱��� © �ʽ�Ź, ���� ���� �� ����� ����>

 EDGC, �������� ���� ��...�ֱǸŸ� �ŷ��Ⱓ�� ����
EDGC, �������� ���� ��...�ֱǸŸ� �ŷ��Ⱓ�� ����