금년들어 식품의약품안전처로부터 임상 3상을 승인 받은 품목은 모두 28개사 32품목인 것으로 나타났다.
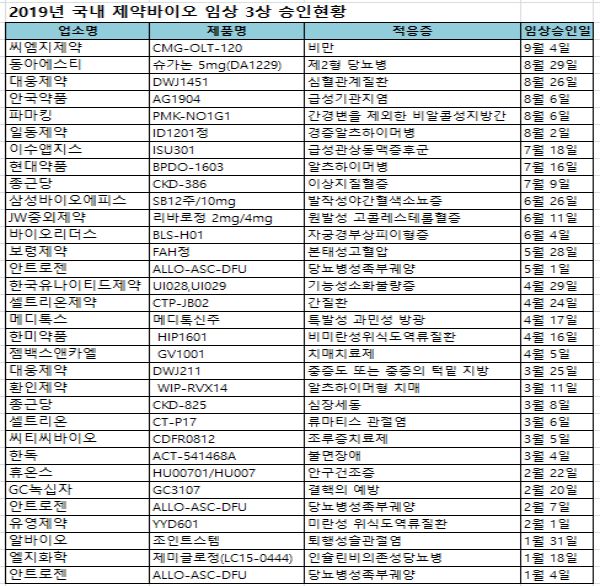 |
임상 3상을 승인 받은 품목들은 개량신약과 복합제,신약등이지만 대부분 복합제가 주류를 이루고 있다.
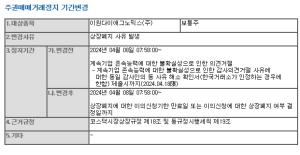
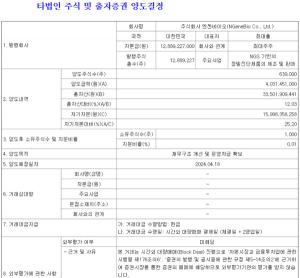
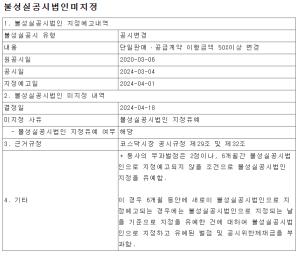
특히 임상 3상 승인 품목중 가장 관심을 끌고 있는 품목은 안트로젠의 당뇨병성족부궤양치료제 ALLO-ASC-DFU, 이수앱지스의 급성관상동맥증후군 치료제 ISU301, 젬백스엔카엘의 GV1001, 알바이오의 조인트스템등이다, 이들 품목들은 글로벌 임상까지 진행하고 있기 때문이다.
안트로젠의 당뇨병성족부궤양치료제 ALLO-ASC-DFU는 3건에 대해 국내 임상 3상을 진행중에 있으며 환자 투약을 시작했고 금년중에 임상을 종료할 계획이다. 특히 당뇨병성족부궤양치료제는 미국에서 임상 2상을 진행하고 있는 것으로 알려졌다.
젬백스앤카엘의 알츠하이머병 치료제 GV1001은 국내 임상 3상 승인뿐 아니라 지난 5월에 미국 식품의약국(FDA)으로부터 2상 임상시험 승인(IND)을 받았다.
GV1001은 인간 텔로머라제에서 유래한 16개 아미노산으로 구성된 펩타이드다. 텔로머라제는 염색체 말단에 존재하는 텔로미어의 길이를 유지하는 고유의 기능 외에 면역 항암, 항염, 항산화, 세포 보호 등의 다양한 기능을 갖고있는 것으로 알려져 있다.
이수앱지스의 혈소판 수용체 차단제 ‘클로티냅주’(ISU 301)는 이번 임상에서 관상동맥중재술(PCI) 시술이 필요한 환자에게 허혈성 심합병증 예방을 위해 항혈전 보조제로 클로티냅주를 투여했을 때 유효성과 안전성을 평가한다.
네이처셀이 주도하고 있는 알바이오의 조인트스템은 6월 강동경희대병원에서 첫 환자가 등록된 임상이 순조롭게 진행되고 있으며 미국 임상은 2상이 완료됐으며, 임상 3상 진행을 위해 FDA와의 협의를 위한 임상시험수탁기관(CRO) 선정을 진행하고 있는 것으로 알려졌다.
종근당의 CKD-386은 고혈압 개량신약이며 CKD-825 고혈압복합제이고 일동제약 ID1201정은 멀구슬나무 열매인 천련자에서 추출한 천연물을 주성분한 천연물치매치료제이다.
현대약품의 BPDO-1603은 치매약으로 사용되는 도네페질과 메만틴 성분을 더한 복합제이며 대웅제약의 심혈관계질환 치료제 DWJ1451은 고혈압과 이상지질혈증을 동반한 환자를 대상으로 임상을 진행중에 있다.
김사랑 기자 kimsarang0420
<저작권자 © 팜스탁, 무단 전재 및 재배포 금지>

 씨엔알리서치-로피바이오, FDA 아일리아 임상 3상 IND 승인
씨엔알리서치-로피바이오, FDA 아일리아 임상 3상 IND 승인